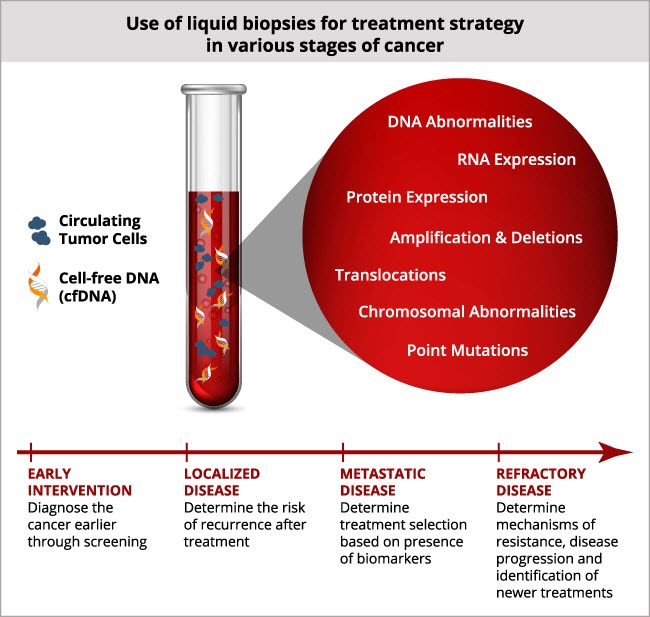
Soluvapaan DNA:n olemassaolo todettiin jo 1940-luvun lopulla, mutta nestebiopsianäytteet (liquid biopsy) ja niiden analysointi on edelleen hyvin akuutti tutkimusaihe, etenkin diagnostisen hyödynnettävyytensä ansiosta.
Mitä nestebiopsiat ovat ja mitä niistä tutkitaan?
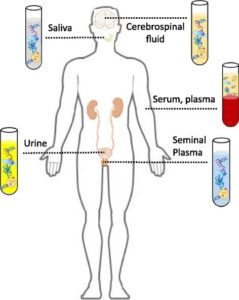 Nestebiopsianäytteillä tarkoitetaan useimmiten ihmisen laskimoverinäytteitä, eli seerumia tai plasmaa. Myös muita kehon nesteitä voidaan käyttää näytemateriaalina, esim. virtsa, selkäydinneste (likvori), sylki, ym. Nämä sisältävät runsaasti erilaisia biomarkkereiksi kelpaavia molekyylejä.
Nestebiopsianäytteillä tarkoitetaan useimmiten ihmisen laskimoverinäytteitä, eli seerumia tai plasmaa. Myös muita kehon nesteitä voidaan käyttää näytemateriaalina, esim. virtsa, selkäydinneste (likvori), sylki, ym. Nämä sisältävät runsaasti erilaisia biomarkkereiksi kelpaavia molekyylejä.
Veressä kiertäviä biomarkkereita on esimerkiksi soluvapaa/solunulkoinen DNA (cell-free DNA, cfDNA) sekä solunulkoisten vesikkelien eli eksosomien sisältämät molekyylit. Syövästä erittyy verenkiertoon ja elimistön muihin nesteisiin myös kiertävää kasvain-DNA:ta ja/tai RNA:ta (circulating tumor DNA ctDNA tai ctRNA) ja kiertäviä kasvainsoluja (circulating tumor cells, CTCs). Soluvapaata DNA:ta erittyy myös muista kehon kudoksista, tai naisen raskaana ollessa, istukasta ja sikiöstä.
Omat haasteensa analysoinnille asettaa kuitenkin näiden markkereiden hyvin pienet pitoisuudet: 10ml kokoveressä genomisen DNA:n osuus on noin 50 µg, josta alle 0,1% (50 ng) on cfDNA:ta. Tästä soluvapaasta DNA:sta puolestaan ctDNA:n osuus on 1-10% eli vain noin 0,5 – 5 ng. Täten esim. syöpäsoluista peräisin oleva DNA edustaa vain murto-osaa soluvapaan DNA:n kokonaismäärästä. Lisäksi, huomionarvoista on myös solunulkoisen DNA:n lyhyt puoliintumisaika joka on vain minuutteja tai tunteja.
Miksi nestebiopsiat?
Nestebiopsiat ovat non-invasiivinen näytemateriaali. Potilasnäyte voidaan kerätä helposti verinäytteenoton yhteydessä, eikä kiinteää kudos/koepalaa tai solunäytettä esim. keuhkosyövän tai aivokasvaimen ollessa kyseessä tarvita.
Jokaisen potilaan kasvain on erilainen, ja jokaisessa kasvaimessa voi olla erilaisia solutyyppejä eli syövät ovat hyvin heterogeenisiä. Kasvainnäytteiden/kudosbiopsioiden sijaan nestebiopsiat edustavat taudin koko profiilia ja täten saadaan analysoitua kokonaistilannetta. Esimerkiksi ctDNA:n määrä vaihtelee taudin eri vaiheissa ja ctDNA:ssa olevia patogeenisiä mutaatioita voidaan analysoida ja hyödyntää syövän diagnostiikassa, seurannassa ja hoitovasteen arvioinnissa.
Mitä näytteenkäsittelyssä kannattaa huomioida?
Parhaan lopputuloksen varmistamiseksi, verinäyte on olennaista kerätä tähän tarkoitukseen soveltuviin putkiin, jotka varmistavat soluvapaan DNA:n ja RNA:n optimaalisen säilymisen. Nukleiinihapot on myös saatava eristettyä menestyksekkäästi jatkoanalyysejä, esim. geenitestejä ja mutaatiotestausta varten.
Nestebiopsiat ja NGS
Tähän mennessä nestebiopsioita on useimmiten analysoitu PCR-pohjaisten menetelmien, kuten digital droplet PCR-tekniikan (ddPCR) avulla. ddPCR:llä nestebiopsioista pystyttiin ensimmäistä kertaa tunnistamaan harvinaista aivokasvaintyyppiä sairastavilta lapsilta genomiset, syöpään liittyvät muutokset (liquid biopsy childhood brain tumors). Tässä tutkimuksessa invasiivista kudosnäytettä ei siis tarvittu lainkaan, vaan löydös ja assosiaatio syöpään oli merkittävä juuri tässä näytetyypissä.
PCR-pohjaisten menetelmien lisäksi nestebiopsianäytteitä voidaan analysoida myös uuden sukupolven sekvensoinnilla eli NGS:llä. Tämä metodi ja sen luotettava hyödyntäminen on aktiivisen kehitystyön alla. Genomisen datan analysoinnissa ja geenimuutoksia tutkittaessa, tärkeä kriteeri on käytettävän menetelmän detektioherkkyys. Nestebiopsianäytteistä detekoitavaa markkeria (esim. CTC) on haastavaa tunnistaa sen vähyyden vuoksi. Siksi muutosten tunnistaminen vaatii kudosnäytteitä suurempaa sekvensointisyvyyttä ja edellyttää myös bioinformatiikan optimointia. NGS:ssä hyväksi todettu detektioherkkyys on mutaation 1-2 prosentin alleelifrekvenssi, mutta menetelmällä on mahdollista päästä käsiksi vielä alhaisempiin frekvensseihin.
Erityisesti MID/UMI:a (unique molecular identifiers) hyödynnettäessä NGS:llä on mahdollista tunnistaa genomisia muutoksia, joiden alleelifrekvenssi on vain 0,1%. Tästä esimerkkinä Paragon Genomicsin UMI Lung cancer paneeli tai Swift Biosciences HS High Sensitivity Panel. Paragon Genomicsin UMI-paneeleita on pian saatavilla myös räätälöityinä, mikä mahdollistaa esimerkiksi laajat tuumorimutaatiotaakka (tumor mutation burden TMB) analyysit erilaisista syöpätyypeistä tai potilaalta syövän eri vaiheissa.
Esimerkiksi, Bolivar et al. hyödynsivät menestyksekkäästi räätälöityä Swift Biosciences NGS-paneelia kohdun limakalvon syöpää sairastavilla potilailla ja pystyivät tunnistamaan ko. syöpään assosioituneet mutaatiot näiden potilaiden plasmanäytteiden cfDNA:sta.
Targetoidut ja juuri nestebiopsianäytteille optimoidut amplikonipohjaiset NGS-paneelit soveltuvat siis erinomaisesti cfDNA:n tai ctDNA:n genomisten muutosten analysointiin ja mahdollistavat harvinaisempienkin varianttien tunnistamisen spesifisesti ja kustannustehokkaasti.
Jos aihe kiinnostaa sinua, kerron mielelläni lisää! Tutustu myös NGS-perusteet blogikirjoitussarjan kirjoituksiin.
Blogin kirjoitti Sanna Siltanen, PhD.